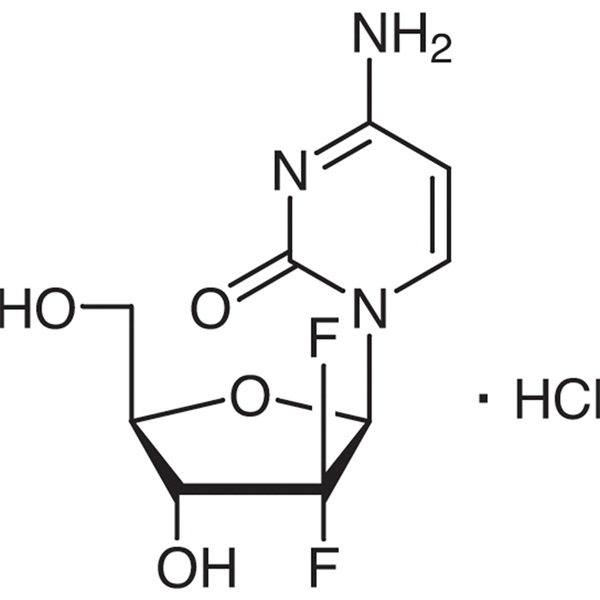
Гемцитабина гидрохлорид CAS 122111-03-9 Стандарт API USP35
Ruifu Chemical является ведущим производителем гемцитабина гидрохлорида (CAS: 122111-03-9) с высококачественной коммерческой продукцией. Ruifu Chemical может обеспечить доставку по всему миру, конкурентоспособные цены, отличный сервис, небольшие и оптовые партии. Купите гемцитабина гидрохлорид, Пожалуйста, свяжитесь с: alvin@ruifuchem.com
| Химическое название | Гемцитабина гидрохлорид |
| Синонимы | гемцитабин гидрохлорид; 2’-дезокси-2’,2’-дифторцитидина гидрохлорид; dFdC; dFdCyd; Гемзар; LY188011 Гидрохлорид; Гемситера; Гемсар |
| Номер CAS | 122111-03-9 |
| Связанный CAS | 95058-81-4 - Бесплатная база |
| Статус запасов | В наличии, производственная мощность 5 тонн |
| Молекулярная формула | C9H12ClF2N3O4 |
| Молекулярный вес | 299,66 |
| Точка плавления | >250℃ |
| Условия доставки | При температуре окружающей среды |
| Сертификат подлинности и паспорт безопасности материала | Доступно |
| Происхождение | Шанхай, Китай |
| Бренд | Руифу Кемикал |
| Товар | Технические характеристики | Результаты |
| Внешний вид | Белый кристаллический порошок без запаха | Соответствует |
| Растворимость | Растворим в воде, слабо растворим в метаноле, практически нерастворим в ацетоне | Соответствует |
| Идентификация ИР | ИК-спектр должен соответствовать эталонного стандарта | Соответствует |
| Идентификация Хлорид | Позитивный. Соответствует требованиям испытаний на хлориды. | Соответствует |
| Внешний вид решения | Раствор S прозрачный и не более интенсивный. цветнее, чем эталонный раствор BY7 | Соответствует |
| pH | 2,0~3,0 | 2.6 |
| Удельное вращение [α]20/D | от +43,0° до +50,0° | +47,5° |
| Тяжелые металлы (Pb) | ≤10 частей на миллион | <10 частей на миллион |
| Потери при сушке | ≤1,00% | 0,3% |
| Остаток при зажигании | ≤0,10% | 0,03% |
| Родственные вещества | ||
| Цитозин | ≤0,10% | 0,01% |
| α-изомер | ≤0,10% | 0,01% |
| Любая другая примесь | ≤0,10% | 0,04% |
| Всего примесей | ≤0,20% | 0,1% |
| Остаточные растворители | ||
| Метанол | ≤0,30% | Не обнаружен |
| Толуол | ≤0,01% | Не обнаружен |
| дихлорметан | ≤0,01% | Не обнаружен |
| Ацетон | ≤0,50% | 0,1% |
| анализ | 97,5%~101,5% (в пересчете на высушенную основу) | 99,9% |
| Заключение | Соответствует стандарту USP35 | |
Пакет: Бутылка, мешок из алюминиевой фольги, картонный барабан по 25 кг или по требованию заказчика.
Условия хранения: Держите контейнер плотно закрытым и храните в прохладном, сухом и хорошо вентилируемом складе вдали от несовместимых веществ. Избегайте воздействия прямых солнечных лучей, влаги и чрезмерного тепла.
Доставка: Доставка по всему миру самолетом с помощью FedEx/DHL Express. Обеспечьте быструю и надежную доставку.

Коды риска R21 - Вреден при попадании на кожу.
Р36/38 - Раздражает глаза и кожу.
Р46 - Может вызвать наследственные генетические повреждения
Р62 - Возможный риск нарушения фертильности
Р63 - Возможный риск причинения вреда будущему ребенку
Описание безопасности S25 - Избегайте попадания в глаза.
С26 - При попадании в глаза немедленно промыть большим количеством воды и обратиться к врачу.
С36/37 - Надевайте подходящую защитную одежду и перчатки.
С53 - Избегайте воздействия - перед использованием получите специальные инструкции.
ВГК Германия 3
РТЕКС HA3840000
Код ТН ВЭД 2942000000
Гемцитабина гидрохлорид (CAS: 122111-03-9) представляет собой новый синтетический дифторнуклеозидный препарат, обладающий антиметаболическими и противоопухолевыми свойствами. Он исследован и разработан компанией Eli Lilly and Company и одобрен для включения в список в Южной Африке, Швеции, Нидерландах, Австралии и других странах в 1995 году. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило его в качестве терапии первой линии для клинического лечения немелкоклеточного рака легких и рака поджелудочной железы.
В последние годы такие новые препараты, как гемцитабин, паклитаксел, доцетаксел, виноребин, являются эффективными препаратами для лечения немелкоклеточного рака легкого (сокращенно НМРЛ). По сравнению с традиционными химиотерапевтическими препаратами эти препараты обладают преимуществами высокого лечебного эффекта и низкой токсичности. Гемцитабина гидрохлорид представляет собой антиметаболитный препарат нового поколения и тип специального лекарства для клеточного цикла, играющего важную роль в фазе синтеза ДНК, а именно в S-фазе клеток. При определенных условиях это лекарство может предотвратить прогрессирование клеток из фазы G1 в фазу S и обладать сильной противораковой активностью при немелкоклеточном раке легких (НМРЛ). Зарубежные исследования показали, что эффективность однократного лечения НМРЛ только гемцитабина гидрохлоридом составляет около 18-35%, тогда как в сочетании с лечением цисплатином эффективность НМРЛ составляет 41,7%. При распространенном НМРЛ эффективность карбоплатина составляет 16%, что аналогично цисплатину, но имеет низкую токсичность, особенно в отношении желудочно-кишечных реакций, подавления костного мозга и токсической реакции почек и нервных окончаний. В сочетании с карбоплатином они оба обладают взаимным координационным и аддитивным действием и могут оказывать более высокий лечебный эффект.
Гемцитабина гидрохлорид
C9H11F2N3O4·HCl 299,66
Цитидин, 2'-дезокси-2',2'-дифтор-, моногидрохлорид.
2'-Дезокси-2',2'-дифторцитидина моногидрохлорид (β-изомер) [122111-03-9].
» Гемцитабина гидрохлорид содержит не менее 97,5 процентов и не более 101,5 процентов C9H11F2N3O4·HCl, рассчитанных на основе «как есть».
[Внимание - Гемцитабина гидрохлорид является мощным цитотоксическим агентом. Следует проявлять особую осторожность, чтобы не вдыхать частицы и не подвергать их воздействию на кожу.]
Упаковка и хранение-Консервы в герметичных емкостях.
Маркировка-Если он предназначен для использования при приготовлении инъекционных лекарственных форм, на этикетке указывается, что он стерилен или должен быть подвергнут дальнейшей обработке во время приготовления инъекционных лекарственных форм.
Справочные стандарты USP<11>-
Фармакопея США Цитозин RS
USP Эндотоксин RS
USP гемцитабина гидрохлорид RS
Идентификация-
A: Инфракрасное поглощение<197K>.
B: Соответствует требованиям испытаний на хлориды<191>.
Удельное вращение<781S>: от +43 до +50, при 20.
Тестовый раствор: 10 мг на мл.
pH<791>: от 2,0 до 3,0, в растворе, содержащем 10 мг на мл.
Остаток при прокаливании<281>: не более 0,1%.
Тяжелые металлы, Метод I<231>: 0,001%.
Хроматографическая чистота-
Решение А - Действуйте, как указано для мобильной фазы анализа.
Раствор B-Приготовьте отфильтрованный и дегазированный метанол.
Подвижная фаза - Используйте переменные смеси растворов A и B, как указано в разделе «Хроматографическая система». При необходимости внесите коррективы (см. «Пригодность системы», раздел «Хроматография 621»).
Раствор для проверки пригодности системы - Действуйте, как указано в анализе.
Стандартный раствор - Растворите точно взвешенное количество гемцитабина гидрохлорида USP и цитозина RS USP в воде и разбавьте количественно, а при необходимости поэтапно, чтобы получить раствор с известной концентрацией около 2 мкг на мл каждого из них.
Испытательный раствор - Перенесите примерно 50 мг гемцитабина гидрохлорида (точно взвешенного) в мерную колбу емкостью 25 мл, растворите в ней воду, разбавьте ее до нужного объема и перемешайте.
Хроматографическая система (см. Хроматография 621)-Действуйте, как указано в разделе «Анализ». Хроматограф программируют следующим образом.
Время (минуты) Раствор А (%) Раствор Б (%) Элюирование
0–8 97 3 изократический
8–13 97®50 3®50 линейный градиент
13–20 50 50 изократический
20–25 50®97 50®3 восстановление равновесия
Хроматографируйте раствор пригодности системы и записывайте пиковые ответы, как указано в процедуре: относительное время удерживания составляет около 0,5 для аномера гемцитабина и 1,0 для гемцитабина; разрешение R между аномером гемцитабина и гемцитабином составляет не менее 8,0; а хвостовой фактор для гемцитабина не превышает 1,5. Хроматографируйте стандартный раствор и записывайте пиковые ответы, как указано в процедуре: относительное время удерживания составляет около 0,1 для цитозина и 1,0 для гемцитабина; относительное стандартное отклонение для повторных инъекций составляет не более 2,0%.
Процедура - Отдельно введите объем (около 20 мкл) стандартного раствора и тестируемого раствора в хроматограф, запишите хроматограмму и измерьте все пиковые реакции. Рассчитайте процентное содержание цитозина в принятой порции гемцитабина по формуле:
2,5(Cc/W)(rt/rs)
где Cc — концентрация цитозина RS согласно Фармакопее США в стандартном растворе, мкг на мл; W — масса принятого гемцитабина, мг; rt — пик реакции на цитозин в тестируемом растворе; rs – реакция на цитозин в Стандартном растворе: цитозина обнаружено не более 0,1%. Рассчитайте процентное содержание каждой примеси, кроме цитозина, в принятой порции гемцитабина по формуле:
2,5(Cs/W)(ri/rs)
где Cs — концентрация гемцитабина гидрохлорида USP RS в стандартном растворе, мкг на мл; W — масса принятого гемцитабина, мг; ri — пиковый отклик для каждой примеси в тестируемом растворе; rs — реакция на гемцитабин в Стандартном растворе: обнаруживается не более 0,1% аномера гемцитабина или любой другой индивидуальной примеси; а сумма всех примесей не более 0,2%. Исключите из суммы всех примесей любые пики, находящиеся ниже предела количественного определения (0,02%).
Другие требования - Если на этикетке указано, что гемцитабина гидрохлорид стерилен, он соответствует требованиям по бактериальным эндотоксинам и стерильности, предъявляемым к гемцитабину для инъекций. Если на этикетке указано, что гемцитабина гидрохлорид необходимо подвергнуть дальнейшей обработке при приготовлении инъекционных лекарственных форм, он соответствует требованиям к бактериальным эндотоксинам, указанным в разделе «Гемцитабин для инъекций».
анализ-
Подвижная фаза - Приготовьте профильтрованный и дегазированный раствор, содержащий 13,8 г одноосновного фосфата натрия и 2,5 мл фосфорной кислоты в 1000 мл воды. [примечание-РН этого раствора составляет от 2,4 до 2,6. ]
Раствор для проверки пригодности системы - Перенесите около 10 мг гемцитабина гидрохлорида в небольшой флакон, добавьте 4 мл раствора, содержащего 168 мг гидроксида калия на мл метанола, плотно закройте крышкой и обработайте ультразвуком. Нагревайте при температуре 55°С в течение 6–16 часов, дайте остыть и перенесите содержимое в мерную колбу емкостью 100 мл, последовательно промывая 1% (по объему) фосфорной кислотой. Разбавьте 1% фосфорной кислотой до необходимого объема и перемешайте. [примечание-Этот раствор содержит около 0,02 мг на мл α-аномера гемцитабина.]
Стандартное приготовление - Растворите точно взвешенное количество USP гемцитабина гидрохлорида RS в воде и разбавьте количественно, а при необходимости поэтапно, водой, чтобы получить раствор с известной концентрацией около 0,1 мг на мл.
Подготовка к анализу - Перенесите около 20 мг гемцитабина гидрохлорида, точно взвешенного, в мерную колбу емкостью 200 мл, растворите в ней, разбавьте водой до нужного объема и перемешайте.
Хроматографическая система (см. Хроматография<621>)-Жидкостный хроматограф оснащен детектором 275-нм и колонкой размером 4,6-мм × 25-см, содержащей насадку L7 5-мкм. Скорость потока составляет около 1,2 мл в минуту. Хроматографируйте раствор пригодности системы и записывайте пиковые ответы, как указано в процедуре: разрешение R между аномером гемцитабина и гемцитабином составляет не менее 8,0; а фактор хвоста, определенный по гемцитабину, составляет не более 1,5. Хроматографируйте стандартный препарат и записывайте пиковые ответы, как указано в процедуре: относительное стандартное отклонение для повторных инъекций составляет не более 1,0%.
Процедура - Отдельно введите в хроматограф равные объемы (около 20 мкл) стандартного препарата и препарата для анализа, запишите хроматограммы и измерьте отклики основных пиков. Рассчитайте количество, в мг, C9H11F2N3O4·HCl в взятой порции гемцитабина гидрохлорида по формуле:
200С(РУ/РС)
где C — концентрация гемцитабина гидрохлорида RS в мг на мл в стандартном препарате; и rU и rS представляют собой пиковые ответы, полученные от препарата для анализа и стандартного препарата, соответственно.